Calcifilaxis en una paciente en hemodiálisis: complicación grave con elevada mortalidad
María Pilar Cardona-Blasco, Elena Liset Cahuancama-Solano, Eva Elías-Sanz
Servicio de Hemodiálisis. Hospital Clínic de Barcelona. España
https://doi.org/10.37551/S2254-28842023018
Como citar este artículo:
Cardona-Blasco MP, Cahuancama-Solano EL, Elías-Sanz E.
Calcifilaxis en una paciente en hemodiálisis: complicación grave con elevada mortalidad. Enferm Nefrol 2023;26(2):178-84
Correspondencia:
|
Recepción: 08-04-2023
|
RESUMEN
Descripción del caso: Paciente con enfermedad renal crónica terminal en tratamiento de hemodiálisis desde hace 1 año. Acude a sesión de hemodiálisis refiriendo lesiones cutáneas muy dolorosas con aspecto necrótico de 2 semanas de evolución en extremidades inferiores distales sugestivas de calcifilaxis. Dados los antecedentes clínicos de fibrilación auricular paroxística, anticoagulada con acenocumarol y los factores de riesgo que presenta, se inician medidas inmediatas dado el mal pronóstico de dicha enfermedad.
Descripción/evaluación del plan de cuidados: Se suspende tratamiento con acenocumarol iniciando anticoagulación con heparina de bajo peso molecular, también se suspenden los suplementos de vitamina D. Se inicia administración de bifosfonatos como inhibidores del calcio, de tiosulfato de sodio como vasodilatador y quelante del fósforo. Se instaura pauta de analgesia siendo uno de los objetivos más importantes del plan de cuidados, el control del dolor, con la administración de opiáceos, antiinflamatorios no esteroideos o mórficos. Aunque fue de difícil manejo, el papel de enfermería ha sido fundamental para procurar el máximo confort. También fue muy importante la vigilancia y el cuidado de las lesiones para prevenir infecciones y controlar la enfermedad observándose una adversa y rápida evolución a pesar de las terapias coadyuvantes, puesto que cuando se diagnosticó ya presentaba lesiones necróticas.
Conclusiones: La calcifilaxis es una complicación poco frecuente pero grave que suele observarse en pacientes con enfermedad renal crónica, sobre todo en hemodiálisis. El tratamiento es multidisciplinar y es importante identificar precozmente a estos pacientes. Desgraciadamente, como en nuestro caso, los resultados no son siempre favorables.
Palabras clave: calcifilaxis; enfermedad renal crónica; hemodiálisis; planes de atención en enfermería; atención de enfermería.
ABSTRACT
Calciphylaxis in a hemodialysis patient: a serious complication with high mortality
Case description: Patient with end-stage renal disease undergoing hemodialysis treatment for 1 year. The patient presents to the hemodialysis session with extremely painful necrotic-looking skin lesions on the distal lower extremities, suggestive of calciphylaxis, which have been present for 2 weeks. Given the patient’s medical history of paroxysmal atrial fibrillation and anticoagulation with acenocoumarol, along with the risk factors present, immediate measures are initiated due to the poor prognosis of this condition.
Description/evaluation of the care plan: Acenocoumarol treatment is discontinued, and anticoagulation with low molecular weight heparin is initiated. Vitamin D supplements are also discontinued. Bisphosphonates are started as calcium inhibitors, sodium thiosulfate is administered as a vasodilator, and phosphate binder. An analgesic regimen is established, with pain control being one of the most important goals of the care plan. This includes the administration of opioids, nonsteroidal anti-inflammatory drugs, or morphine. Although challenging, the nursing role has been crucial in providing maximum comfort. Close monitoring and wound care are also important to prevent infections and control the disease, although an adverse and rapid progression was observed despite the adjunctive therapies, as necrotic lesions were already present at the time of diagnosis.
Conclusions: Calciphylaxis is a rare but serious complication often observed in patients with chronic kidney disease, especially in those undergoing hemodialysis. Treatment is multidisciplinary, and early identification of these patients is important. Unfortunately, as in our case, the outcomes are not always favorable.
Keywords: calciphylaxis; chronic kidney disease; hemodialysis; nursing care plans; nursing care.
INTRODUCCIÓN
La calcifilaxis o arteriolopatía urémica calcificante es un síndrome clínico caracterizado por la ulceración necrótica de la piel debida a la calcificación de la capa media, más fibrosis de la íntima arteriolar y posterior isquemia cutánea por trombosis1. Selye describe la calcifilaxis por primera vez en 1962 y todavía no hay un tratamiento específico2. Los pacientes con enfermedad renal crónica (ERC) sufren de hipocalcemia, lo cual provoca una hiperfosforemia, agravada en estos pacientes por la dificultad del aclaramiento por su insuficiencia renal. Esto incita a la transformación de las células del músculo liso vascular en células similares a los osteoblastos3. Afecta principalmente a los pacientes en hemodiálisis (HD) con una tasa de incidencia de 0,04% en Europa, aunque también puede afectar a pacientes con función renal normal4. Otros factores de riesgo además del tiempo en terapia sustitutiva renal, es el sexo femenino, la diabetes mellitus, la raza caucásica y la inflamación crónica; y como factores modificables destacarían la obesidad, la desnutrición, la hiperfosforemia, el hiper o hipoparatiroidismo, la anticoagulación con antagonistas de la vitamina K y el estado de hipercoagulabilidad1.
Las manifestaciones clínicas empiezan por una decoloración violácea de la piel, progresan a placas y pueden ulcerarse rápidamente. Se presentan a nivel distal o proximal en las extremidades inferiores (EEII), siendo más grave cuando aparecen las lesiones en tronco, nalgas y muslos1.
El diagnóstico es básicamente clínico. Cuando un paciente en ERC presenta placas dolorosas e induradas o úlceras en el abdomen y/o piernas ya hace sospechar de calcifilaxis. Se puede respaldar con pruebas radiológicas, siendo la biopsia de piel el método estandarizado para un diagnóstico definitivo5. Otras pruebas que ayudarían al diagnóstico serían gammagrafía ósea, mamografía y radiografías.
Tiene una tasa de mortalidad entre 30-80%, básicamente por la sobreinfección de las lesiones, el difícil control del dolor y los requerimientos de hospitalización4.
Describimos el caso de una paciente con enfermedad renal crónica terminal (ERCT) en HD que presentó, tras un año de tratamiento, calcifilaxis en los miembros inferiores distales bilateralmente.
PRESENTACIÓN DEL CASO
Mujer de 78 años, sin alergias conocidas ni hábitos tóxicos, independiente para las actividades de la vida diaria (ABVD), ingresada en residencia tras fractura humeral derecha en marzo del 2021. Con antecedentes clínicos de:
- Diabetes Mellitus (DM) tipo 2.
- Hipertensión arterial (HTA).
- Dislipemia.
- Obesidad moderada.
- Cardiopatía isquémica desde 2016, en tratamiento con antiagregantes.
- Suprarrenalectomía izquierda en 2014 por mielolipoma y resección transuretral por carcinoma urotelial. Cuatro años después se realiza nefro-ureterectomía izquierda, cistectomía y colocación de catéter J en nefrostomía derecha, ooforectomía y salpingectomía bilateral.
- ERCT desde 2018.
- Fibrilación auricular paroxística anticoagulada con acenocumarol desde febrero de 2019.
- Apnea obstructiva del sueño (AOS).
- Mieloma múltiple en julio 2020.
- Fractura humeral derecha tras caída y colocación de catéter venoso central (CVC) tunelizado en marzo del 2021 para inicio de HD.
Tras un año en HD acude a urgencias derivada por nuestro centro al presentar lesiones cutáneas necróticas muy dolorosas de dos semanas de evolución en EEII con sospecha de calcifilaxis, en abril del 2022. Se sustituye acenocumarol por heparina de bajo peso molecular (HBPM) de acuerdo con hematólogo, se programan sesiones de HD con administración en tres sesiones de pamidronato 60 mg endovenoso cada quince días y se instaura pauta de analgesia con paracetamol más antiinflamatorios no esteroideos (AINES), neuromodeladores y mórficos de rescate. Se confirma diagnóstico en las imágenes de mamografía bilateral en EEII.
En el mes de junio presenta mala tolerancia a los opiáceos y sobreinfección de las lesiones requiriendo antibioticoterapia e ingreso hospitalario. Se añade tiosulfato sódico al tratamiento y sesiones diarias de HD. Las lesiones van en aumento y se contacta con cirugía general no recomendando desbridamiento. Los cirujanos vasculares determinan ausencia de patología macrovascular. Los cirujanos plásticos no creen que las úlceras sean candidatas a tratamiento quirúrgico e instauran curas con antisépticos y antibióticos tópicos y sugieren consultar con dermatología, los cuales aconsejan desbridamiento y nueva pauta de curas. Sigue seguimiento en la clínica del dolor logrando un mejor control de analgesia con AINES, además de metadona de rescate. En agosto, se aplica terapia de cierre asistido por vacío (VAC), desbridamiento mecánico, fomentos con Prontosan® y apósito de plata. Las radiografías de EEII a mediados de mes, muestran ausencia de afectación ósea. Llegó a presentar sangrado en chorro de una de las heridas requiriendo taponamiento mecánico y administración de ácido tranexámico y posteriormente nuevo sangrado arterial necesitando sutura quirúrgica.
Ese mismo agosto se valora nutricionalmente, orientándose como desnutrición proteica y se inició nutrición enteral (NE) con sonda nasogástrica (SNG) y suplementos orales. A finales de octubre, tras nueva valoración, se cambió por nutrición parenteral intradiálisis (NPID) y se decidió activación de limitación de esfuerzo terapéutico (LET). A principios de noviembre tiene lugar el último ingreso por shock séptico con mal pronóstico, siendo exitus tres días después.
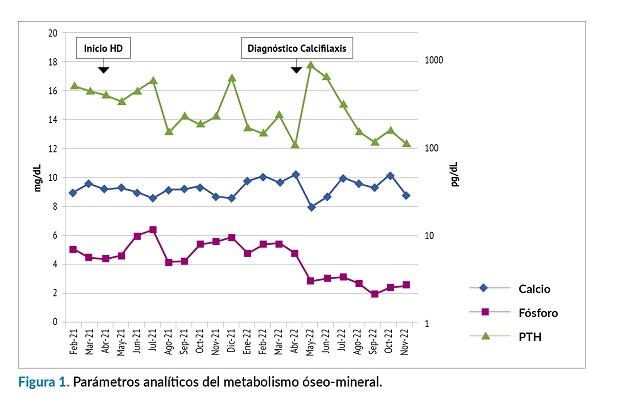
En la figura 1 puede observarse la evolución de los parámetros analíticos del metabolismo óseo-mineral desde el inicio de la terapia con HD.
Valoración enfermera
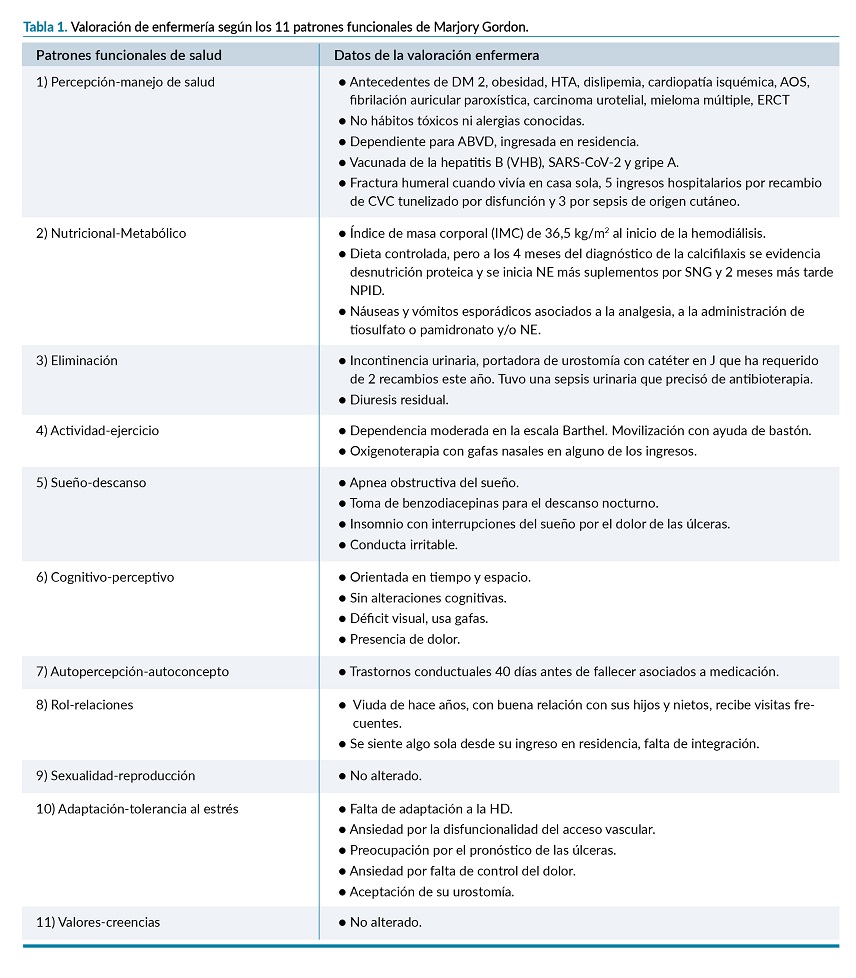
En la tabla 1 se muestra la valoración de enfermería según los once patrones funcionales de Marjory Gordon6.
Plan de cuidados
Planteamos un plan de cuidados utilizando la taxonomía NANDA (North American Nursing Diagnosis Association)7 tras identificar los problemas potenciales de salud, con los objetivos enfermeros utilizando taxonomía NOC (Nursing Outcomes Classification)8 y las intervenciones enfermeras utilizando taxonomía NIC (Nursing Interventions Classification)9 (ver tabla 2).

Evaluación del Plan de Cuidados
Tras seis meses de evolución los resultados no fueron los esperados debido a las complicaciones que se presentaron.
- Dolor crónico. Fue muy difícil el manejo del dolor a pesar del tratamiento farmacológico, siendo el apoyo de enfermería un aspecto fundamental.
- Deterioro de la integridad cutánea. Se monitorizó la evolución de las lesiones tanto en número como en superficie dañada observándose una adversa y rápida evolución a pesar de las terapias coadyuvantes.
- Riesgo de infección. El cuidado del CVC tunelizado fue óptimo y la paciente fue autosuficiente en el cuidado de la ostomía, aunque presentó una infección urinaria. Las lesiones dérmicas asociadas a la calcifilaxis se sobreinfectaron provocando, en su último ingreso, un shock séptico.
- Ansiedad. A pesar de detectar un nivel de ansiedad elevado podríamos decir que se consiguió disminuir dicho nivel favoreciendo que la paciente expresara sus inseguridades y tomara conciencia de las conductas y factores a modificar.
- Náuseas y/o vómitos. Se controlaron con analgesias alternativas y la administración de antieméticos.
- Desequilibrio nutricional por defecto. Se inició NE con suplementos orales para corregir la desnutrición proteica y más tarde NPID, pero no hubo tiempo suficiente para revertir esta complicación.
DISCUSIÓN
Actualmente no existen guías de práctica clínica basadas en la evidencia para la prevención y tratamiento de la calfilaxis. Se están estableciendo registros nacionales sobre calcifilaxis para ayudar a recopilar datos de calidad, tendencias de tratamiento y medidas de eficacia10.
El tratamiento en primera instancia sería manejar el dolor sintomático, ya que parece ser que los componentes isquémicos como los neuropáticos desempeñan un papel fundamental. El dolor es a menudo resistente a los opiáceos y suele ser necesario consultar con la clínica del dolor11.
Otro de los pilares del tratamiento sería modificar factores de riesgo, como medicaciones o comorbilidades que pueden contribuir a su desarrollo: suspendiendo la anticoagulación con antagonistas de la vitamina K y cambiar por HBPM y optimizando la función renal, evitando la hipercalcemia e hiperfosforemia, suspendiendo los suplementos de vitamina D y administrando quelantes de fósforo (P) no cálcicos. Como inhibidores eficaces de la calcificación se están administrando hace unos años, tiosulfato de sodio y biofosfonatos1,11-13. La mayoría de los estudios sugieren aumentar las sesiones de HD4,11,14,15 y modificar el baño de 3 meq a 2,5 meq de Ca4,11 ó a 1,5 meq15, en nuestro caso no fue necesario modificar el Ca y se aumentó la frecuencia a diálisis diarias durante 8 días. El P se normalizó tras iniciar tratamiento con pamidronato y tiosulfato. La PTH estuvo elevada, alcanzando niveles de 875 pg/ml y disminuyendo después.
Es importante el control de las heridas midiéndolas periódicamente, prevención de infecciones, administración de antibióticos, limpieza y asepsia y utilización de apósitos hidrocoloides. Se recomienda un abordaje precoz de las lesiones. En nuestro caso las lesiones aumentaron en extensión y número y se sobreinfectaron requiriendo ingreso hospitalario. El desbridamiento es controvertido por riesgo de infección o hemorragia14. La oxigenoterapia hiperbárica puede favorecer la recuperación de las lesiones necróticas y mantener un buen estado nutricional para favorecer la cicatrización11. Cuatro meses después, la paciente, presenta hipoalbuminemia de 24g/l y se decide iniciar NE más suplementos y en dos meses NPID.
El enfoque de la calcifilaxis es multidisciplinar5,14, participando nefrólogos, dermatólogos, cirujanos plásticos, cirujanos vasculares y dietistas.
A pesar de todo ello, sigue teniendo mal pronóstico y la causa más frecuente de muerte es la sepsis de origen cutáneo15. Distintos estudios muestran que una vez diagnosticada la calcifilaxis, ésta sigue un curso acelerado12. Nuestra paciente murió a los seis meses de la aparición de las primeras lesiones.
Los pacientes con ERCT presentan riesgo elevado de calcifilaxis, por tanto, deberíamos prevenir la progresión de las lesiones y su sobreinfección, optimizando tratamientos e incidiendo en los factores de riesgo modificables. El diagnóstico precoz y un enfoque multidisciplinar son clave para el manejo de esta enfermedad.
BIBLIOGRAFÍA
1. Cucchiari D, Torregrosa J-V. Calcifilaxis en pacientes con enfermedad renal crónica: una enfermedad todavía desconcertante y potencialmente mortal. Nefrologia 2018;38(6):579–86.
2. Selye H. Calciphilaxis. University of Chicago Press; 1962.
3. Karwowski W, Naumnik B, Szczepański M, Myśliwiec M. The mechanism of vascular calcification-a systematic review. Med Sci Monit 2012;18(1):RA1-11.
4. Zoi V, Bacharaki D, Sardeli A, Karagiannis M, Lionaki S. Calciphylaxis: A Long Road to Cure with a Multidisciplinary and Multimodal Approach. Case Reports Nephrol 2022: 3818980.
5. Abdalla AO, Al-Khafaji J, Taha M, Malik S. A fatal case of non-uremic calciphylaxis: A case report and literature review. Am J Case Rep 2018;19:804-7.
6. Gordon M. Manual de diagnósticos enfermeros. 10a. Madrid: Elsevier; 2003.
7. Herdman T, Kamitsuru S, Takáo Lopes C. Diagnósticos enfermeros. Definiciones y clasificación 2021-2023. 12a. Barcelona: Elsevier; 2021.
8. Moorhead S, Swanson E, Johnson M, Maas M. Clasificación de Resultados de Enfermería (NOC): Medición de Resultados en Salud. 6a. Barcelona: Elsevier; 2018.
9. Butcher H, Bulechek G, Dochterman J, Wagner C. Clasificación de Intervenciones de Enfermería (NIC). 7a. Barcelona: Elsevier; 2018.
10. Udomkarnjananun S, Kongnatthasate K, Praditpornsilpa K, Eiam-Ong S, Jaber BL, Susantitaphong P. Treatment of Calciphylaxis in CKD: A Systematic Review and Meta-analysis. Kidney Int Reports 2019;4(2):231–44.
11. Seethapathy H, Brandenburg V, Sinha S, El-Azhary R, Nigwekar S. Review: update on the management of calciphylaxis. QJM 2019;112(1):29–34.
12. Bover J, Ureña-Torres P, Górriz JL, Lloret MJ, da Silva I, Ruiz-García C, et al. Cardiovascular calcifications in chronic kidney disease: Potential therapeutic implications. Nefrologia 2016;36(6):597-608.
13. Cobelo C, García-Enriquez A, González-Tabares L, Cillero S, Quispe J, Otero P, et al. Tiosulfato tópico como tratamiento de calcifilaxis. Nefrologia 2019;39(3):329.
14. Chang J. Calciphylaxis: Diagnosis, Pathogenesis, and Treatment. Adv Ski Wound Care 2019;32(5):205–15.
15. Guzmán UV, De La Cueva P, Verde E, García de Vinuesa S, Goicoechea M, Mosse A, et al. Calcifilaxis: complicación grave del síndrome cardio-metabólico en pacientes con enfermedad renal crónica terminal (ERCT). Nefrologia 2008;28(1):32-6.
Este artículo se distribuye bajo una Licencia Creative Commons Atribución–NoComercial 4.0 Internacional.
https://creativecommons.org/licenses/by-nc/4.0/
