Valoración de la fragilidad en un centro de diálisis. ¿Son más frágiles los pacientes con diabetes?
Sonia Guerrero-Carreño, Eva Elías-Sanz, Miquel Gómez-Umbert, Marta Quintela-Martínez, Teresa Gabarró-Taulé, Marta Arias-Guillén
Centre de Diàlisi i Recerca Aplicada Clínic (DIRAC). Hospital Clínic. Barcelona. España
https://doi.org/10.37551/S2254-28842023003
Como citar este artículo:
Guerrero-Carreño S, Elías-Sanz E, Gómez-Umbert M, Quintela-Martínez M, Gabarró-Taulé T, Arias-Guillén M.
Valoración de la fragilidad en un centro de diálisis. ¿Son más frágiles los pacientes con diabetes?
Enferm Nefrol 2023;26(1):24-32
Correspondencia:
|
Recepción: 20-03-2022
|
RESUMEN
Introducción: El incremento en la inclusión de personas de edad avanzada a los programas de hemodiálisis se relaciona con un aumento de la prevalencia de fragilidad, considerada predictora de discapacidad y asociada a eventos adversos de salud. Dado su carácter reversible, es importante hacer un cribaje para mejorar la práctica clínica.
Objetivo: Evaluar el grado de fragilidad y estado funcional del paciente en nuestra unidad de hemodiálisis y analizar las diferencias entre diabéticos y no diabéticos.
Material y Método: Estudio observacional de corte transversal. La fragilidad se midió utilizando el fenotipo de Fried y la valoración funcional mediante las escalas Barthel, Lawton, Downton y la Short Physical Performance Battery. Se evaluó comorbilidad y riesgo de caídas con las escalas Charlson y Downton respectivamente. Se comparó entre grupos de diabéticos y no diabéticos y se analizó la relación entre la fragilidad y la edad, dependencia, comorbilidad y riesgo de caídas.
Resultados: Se incluyeron 128 pacientes. El 45% tenían Diabetes. Los pacientes con diabetes tenían una edad media mayor que los no diabéticos (74,2±11 vs 67,8±15 años) y mayor comorbilidad (Charlson 8,2±2,2 vs 5,8±2,4). El 25% de los pacientes presentaron fragilidad, observando una tendencia que sugirió mayor fragilidad, peor capacidad funcional y mayor grado de dependencia en los pacientes diabéticos, aunque de forma no significativa.
Conclusiones: Una cuarta parte de la población estudiada presenta fragilidad, con una tendencia más acusada a padecerla los pacientes diabéticos, que podría estar relacionada con mayor edad, mayor comorbilidad y menor capacidad funcional que los no diabéticos.
Palabras clave: diabetes mellitus; insuficiencia renal crónica; fragilidad; hemodiálisis.
ABSTRACT
Fragility assessment in a dialysis center. Are patients with diabetes more fragile than others?
Introduction: The increase in the inclusion of elderly people in hemodialysis programs is connected to a rise in the prevalence of their frailty, considered as well as a prediction of disability and often associated with adverse health events. Given its reversible nature, screening is essential to improve clinical practice.
Objective: To assess the frailty index and the patient functional status in our hemodialysis unit, as well as analyze the differences between diabetics and non-diabetics.
Material and Method: Observational cross-sectional study. Frailty was measured using the Fried phenotype and functional assessment using the Barthel, Lawton, Downton, and Short Physical Performance Battery scales. Comorbidity and fall risk were evaluated with the Charlson and Downton scales, respectively. Diabetic and non-diabetic groups were compared, as well as the relationship between frailty and age, dependency, comorbidity, and fall hazard was analyzed.
Results: A hundred and twenty-eight patients were included in the study. 45% had diabetes. Diabetic patients had a higher average age than non-diabetics (74.2±11 vs 67.8±15 years) and higher comorbidity (Charlson 8.2±2.2 vs 5.8±2.4). Twenty-five percent of the patients had frailty, observing a trend that suggests higher frailty, worse functional capacity, and a higher degree of dependency in diabetic patients, although not significantly.
Conclusions: A quarter of the sampled analyzed presents frailty, with a more pronounced tendency to suffer from it in the case of diabetic patients, which could be related to older age, higher comorbidity, and less functional capacity than non-diabetic people.
Keywords: diabetes mellitus; chronic renal failure; frailty; hemodialysis.
INTRODUCCIÓN
La Enfermedad Renal Crónica (ERC) representa un importante problema de salud pública por su elevada incidencia y prevalencia, su importante morbi-mortalidad y su elevado coste socioeconómico1.
La prevalencia de la ERC en España se sitúa en torno al 15,1%2. Según datos recogidos en 2020 por el Registro Español de Enfermedades Renales (REER), la Diabetes Mellitus (DM) es, actualmente, la principal causa de inicio de tratamiento con Hemodiálisis (HD), siendo la enfermedad renal primaria en el 26% de los casos incidentes y manteniéndose en el 16-17% de los casos prevalentes3.
La elevada prevalencia de ambas patologías junto al envejecimiento de la población, el mejor manejo de las complicaciones cardiovasculares, la mayor flexibilidad en la inclusión de pacientes en HD y la mejora en la tolerancia al tratamiento gracias a los avances tecnológicos, han permitido la entrada en programa de HD a pacientes de edad cada vez más avanzada y con mayor comorbilidad4,5. De forma secundaria, es de suponer que el número de personas con DM que requerirán tratamiento con HD seguirá en aumento3. Esto supondrá un cambio de perfil de nuestros pacientes, en el que la combinación de envejecimiento, ERC y otras patologías concomitantes puede conducir, inevitablemente, al desarrollo de fragilidad6-8.
La fragilidad es un concepto que surge en las últimas 3 décadas como un estado del individuo que precede a la discapacidad pero que, contrariamente a ésta, puede ser reversible9. Este término ha ido evolucionando hasta la publicación en 2013 del Documento de Consenso sobre Fragilidad, donde se definió como un síndrome clínico, de etiología múltiple, caracterizado por una disminución de la fuerza, resistencia y reservas fisiológicas que aumenta la vulnerabilidad de un individuo para desarrollar una mayor dependencia y/o la muerte10.
La relación de la fragilidad con la ERC y la DM ha sido reconocida en otros estudios6,11. Los procesos asociados a la ERC tales como la inflamación y el estrés oxidativo12, la malnutrición y la sarcopenia, la comorbilidad, la enfermedad cerebrovascular y el deterioro cognitivo13, el deterioro funcional14, la anemia y la enfermedad mineral ósea van a contribuir al desarrollo de fragilidad6. La DM también puede desencadenar fragilidad. La pérdida de peso (provocada por estados de hiperglicemia sostenida, gastroparesia o por efectos de algunos fármacos hipoglucemiantes), la resistencia a la insulina (que afecta al funcionamiento de las fibras musculares, provocando debilidad y pérdida muscular) y los posibles episodios de hipoglucemia (que aumentan el riesgo de caídas), favorecen el desarrollo de fragilidad11.
En los pacientes en tratamiento con HD se suman las limitaciones en la actividad física propias del tratamiento y las hipotensiones que ocasionalmente sufren después de finalizar la terapia, que favorecen el riesgo de caídas, aumentando el número de hospitalizaciones y afectando a su calidad de vida y capacidad funcional favoreciendo, a su vez, la aparición de discapacidad9,15.
La coexistencia de ambas patologías en aquellos pacientes especialmente frágiles, como puede ser nuestra población en HD, puede condicionar mayor deterioro funcional y desarrollo de discapacidad16-19.
Esta situación plantea un cambio de escenario en la atención del paciente anciano en HD, más aún si éste presenta DM. En los pacientes ancianos frágiles con múltiples comorbilidades, alto riesgo de hipoglucemias y caídas (como pueden ser los pacientes diabéticos en HD) se ha observado que los beneficios de un buen control glucémico son menores y que el objetivo a cumplir con estos pacientes es prevenir y/o evitar las complicaciones agudas de la DM20. El personal sanitario ha de dar respuesta a las necesidades asistenciales para adecuar los cuidados y minimizar los riesgos, sobre todo en estos pacientes más frágiles.
Por todo esto, se hace imprescindible el cribado de la fragilidad, ya que ha sido señalada por algunos autores como un fuerte predictor de discapacidad, hospitalización, caídas, pérdida de movilidad, enfermedad cardiovascular e incluso la muerte, siendo los individuos más frágiles más vulnerables a estos eventos adversos7,21-23.
La herramienta de cribado más utilizada hasta ahora en pacientes con ERC ha sido la propuesta por Fried y colaboradores en el Cardiovascular Health Study, donde se instauró la base del concepto de fragilidad y se propuso el “Fenotipo de fragilidad” como herramienta de cribado21. En dicho estudio, para catalogar a una persona frágil era necesaria la presencia de, al menos, 3 de estos 5 criterios: pérdida de peso no intencionada, estado de ánimo decaído, actividad física, baja velocidad en la marcha y debilidad muscular.
La detección precoz de la fragilidad en los pacientes en HD identificaría a aquellas personas más vulnerables de presentar problemas de salud para que puedan beneficiarse de medidas preventivas o terapéuticas que reviertan total o parcialmente este estado de fragilidad, motivo por el cual nos planteamos el presente estudio, con el objetivo principal de evaluar el grado de fragilidad y el estado funcional de los pacientes en nuestra unidad de HD; y como objetivo secundario analizar si existían diferencias en el grado de fragilidad y el estado funcional entre los grupos de diabéticos y no diabéticos.
MATERIAL Y MÉTODO
Diseño del estudio: Se ha realizado un estudio observacional descriptivo de corte transversal en la unidad de HD del Hospital Clínico de Barcelona (HCB) y su Centro Periférico de Diálisis e Investigación Aplicada (DIRAC) durante el periodo de seguimiento que comprendió desde marzo de 2019 hasta marzo de 2021.
Población de estudio: Pacientes con ERC estadio 5 que realizan tratamiento con HD en el HCB, así como en su centro periférico DIRAC.
Criterios de inclusión: Estancia mínima de 3 meses en programa de HD, capacidad para comprender y cumplimentar los cuestionarios facilitados o, en su defecto, disponibilidad de familiar o cuidador en caso de dificultad para realizarlos (deterioro cognitivo/barrera idiomática) y firma del consentimiento informado para la participación en el estudio.
Criterios de exclusión: No voluntariedad de participación en el estudio.
Variables de estudio e instrumentos utilizados: Las variables analizadas en este estudio fueron el grado de fragilidad y el estado funcional de los pacientes en nuestra unidad de HD. Se analizaron también variables sociodemográficas (edad y sexo), antropométricas (peso, talla e IMC) y clínicas (presencia de DM y etiología de la ERC), así como el grado de comorbilidad de los pacientes.
El grado de fragilidad se midió según el Fenotipo de Fragilidad de Fried. El estado funcional se evaluó fundamentalmente con la Short Physical Performance Battery (SPPB) y, de forma complementaria, se contemplaron el riesgo de caídas, mediante la Escala Downton y el grado de dependencia, mediante el Índice de Barthel para las actividades básicas de la vida diaria (ABVD) y la escala Lawton para la actividades instrumentales de la vida diaria (AIVD ). El grado de comorbilidad se evaluó mediante el Índice de Comorbilidad de Charlson modificado (ICCm).
Recogida de los datos
Los datos sociodemográficos, antropométricos y de comorbilidad se recogieron mediante la revisión de la historia clínica del paciente con los programas Nefrolink® y SAP®.
Los diferentes cuestionarios utilizados fueron cumplimentados mediante entrevistas con los pacientes durante las sesiones de HD y, según necesidades, con los familiares o cuidador principal.
Se creó un grupo de trabajo multidisciplinar formado por el nefrólogo responsable de la unidad de HD, la fisioterapeuta y el personal de enfermería (una enfermera y una técnico en cuidados auxiliares de enfermería (TCAE) de cada turno de trabajo. Posteriormente se elaboró un checklist de valoración de paciente frágil con las actividades a realizar por cada profesional, consensuando los criterios para la cumplimentación de cada cuestionario y así disminuir la posible variabilidad interobservador. Por un lado, el nefrólogo valoró la comorbilidad con el Índice de Charlson. La TCAE referente de cada turno valoró el riesgo de caídas con la escala Downton y el grado de dependencia para las ABVD con la escala Barthel. La enfermera referente de cada turno valoró el grado de dependencia para las AIVD mediante la escala Lawton y el grado de fragilidad con la escala Fried. Esta escala se cumplimentó conjuntamente con la fisioterapeuta de la unidad. Los criterios relativos a la pérdida de peso, estado de ánimo y actividad física del test Fried fueron recogidos por la enfermera mediante entrevistas con los pacientes. Para valorar los criterios relativos a la velocidad en la marcha y la debilidad muscular, así como para la realización del test SPPB, se citó a los pacientes con la fisioterapeuta del centro antes del inicio de la diálisis.
Los datos recogidos fueron introducidos en una base de datos Excel anonimizada y sometidos a análisis estadístico.
Análisis estadístico
Los datos fueron procesados mediante el programa SPSS versión 20. Se realizó un análisis de los datos sociodemográficos y clínicos de los sujetos de la muestra mediante estadística descriptiva: frecuencias, medidas de tendencia central y de dispersión.
Las variables cuantitativas se presentaron como media ± desviación estándar dada la naturaleza de su distribución normal analizada mediante el test de Kolmogorov-Smirnov. La comparación de los datos cuantitativos entre los grupos de diabéticos y no diabéticos se realizó mediante el test de la t de Student. Las variables cualitativas se presentaron como frecuencias absolutas y porcentajes. La comparación de los datos cualitativos se realizó mediante el test de Chi-cuadrado (χ2). El estudio de las correlaciones entre las variables cuantitativas se realizó mediante el coeficiente de correlación de Pearson. Fue considerado estadísticamente significativo un valor de p<0,05 con un intervalo de confianza del 95%.
Cuestiones éticas
El estudio fue realizado en base al cumplimiento de principios éticos para investigaciones con seres humanos enmarcados en la Declaración de Helsinki (Fortaleza, Brazil, Oct. 2013). Los datos de carácter personal recogidos han sido respetados y protegidos de acuerdo a la Ley Orgánica de Protección de Datos Personales y garantía de los derechos digitales 3/2018 y el Reglamento UE 2016/679 del Parlamento Europeo.
La recogida y análisis de datos para este estudio ha sido posible gracias a la aceptación de un documento, evaluado y aprobado por el Comité de Ética e Investigación del HCB, para el uso de datos en estudios de revisión y observacionales (Reg.HCB/2018/1168). Los pacientes firmaron consentimiento informado previo a la inclusión en el estudio.
RESULTADOS
Fueron seleccionados un total de 132 pacientes, de los cuales 86 fueron hombres (67%) y 42 mujeres (33%). Se excluyeron 4 pacientes por deterioro cognitivo y barrera idiomática, por lo que el análisis final se realizó en 128 pacientes.
El promedio de edad fue de 70,7±14 años. El 45% (n=58) de los pacientes presentaba DM los cuales, además, resultaron tener edad media mayor que los pacientes no diabéticos (74,2±11 vs 67,8±15 años, p<0,01). Los datos de comorbilidad mostraron una puntuación media en el Índice de Charlson de 8,2±2,2 puntos en los pacientes diabéticos frente a 5,8±2,4 puntos de los no diabéticos (p<0,001), constatando comorbilidad alta (>3 puntos) en el total de nuestros pacientes.
Todos los resultados de los diferentes test realizados se muestran en la tabla 1.
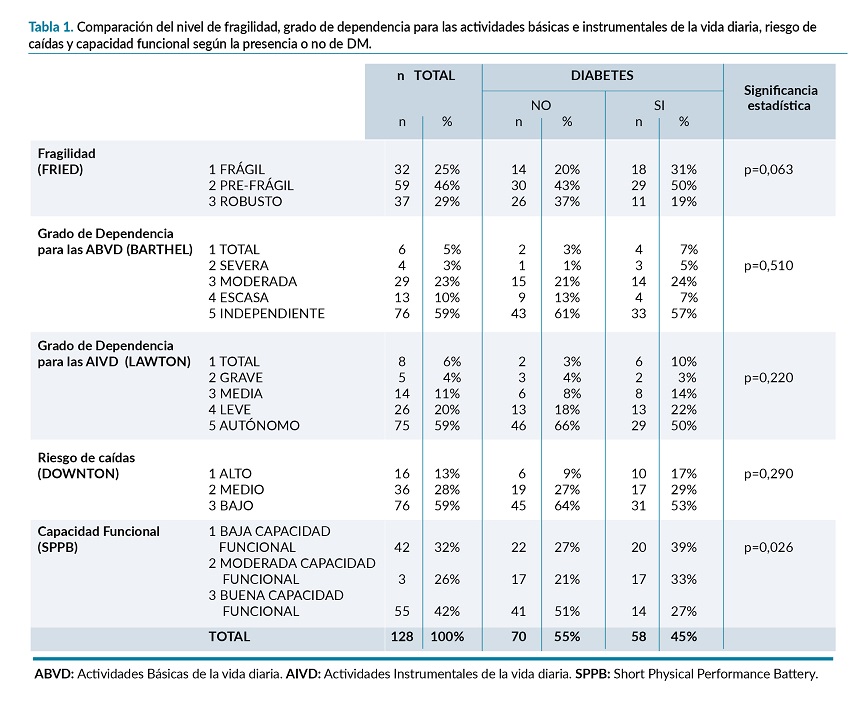
Según el test de Fried, fueron catalogados como frágiles el 25% (n=32) de nuestros pacientes y pre-frágiles el 46% (n=59); Diferenciando entre sexos, el 17% (n=15) de los hombres son frágiles frente al 40% (n=17) de las mujeres.
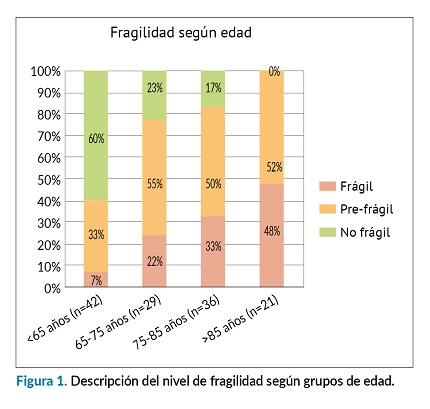
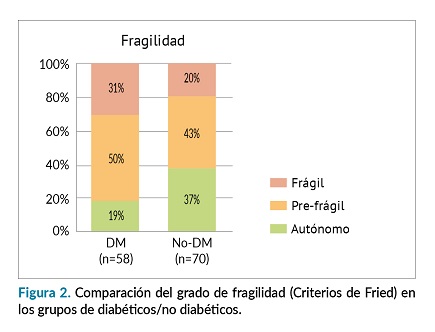
Por franjas de edad, se observa que el 7% (n=3) de los pacientes menores de 65 años son frágiles, así como el 24% (n=7) de los que tienen entre 65-75 años, el 33% (n=12) entre los de 75-85 años y el 48% (n=10) de los mayores de 85 años (figura 1). Comparando la fragilidad entre los grupos de DM/no DM, los pacientes diabéticos resultaron ser porcentualmente más frágiles o prefrágiles que los no diabéticos (81% DM vs 63% no DM) (figura 2).
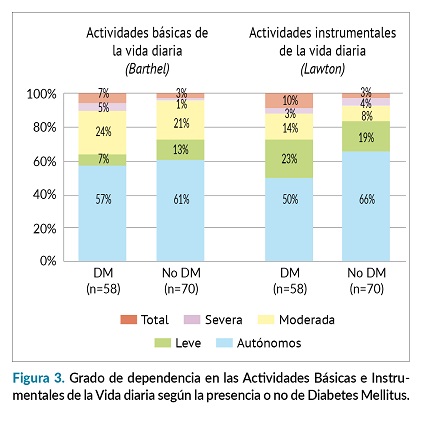
Respecto a las ABVD, el 8% (n=10) de los pacientes presentaron dependencia severa-total. Comparando los grupos diabéticos/no diabéticos, se observa un mayor porcentaje de dependencia severa-total en pacientes diabéticos (12% DM vs 4% no DM) y un mayor porcentaje de pacientes autónomos en el grupo de no diabéticos. Por otro lado, el 10% (n=13) de los pacientes presentaron dependencia severa-total para las AIVD y moderada el 11% (n=14). Ambos test parecen mostrar una tendencia que indica mayor dependencia del grupo de diabéticos para las actividades básicas e instrumentales de la vida diaria (ABIVD), pero sin alcanzar en ninguno de los casos la significancia estadística (figura 3).
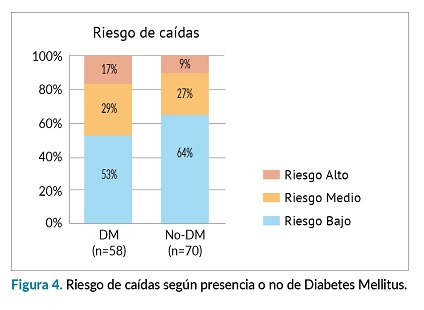
Según la escala Downton, el 13% (n=16) de los pacientes tienen un riesgo alto de caídas, siendo mayor en mujeres que en hombres (16% vs 10%) y en pacientes diabéticos frente a los no diabéticos (17% vs 9%) (figura 4).
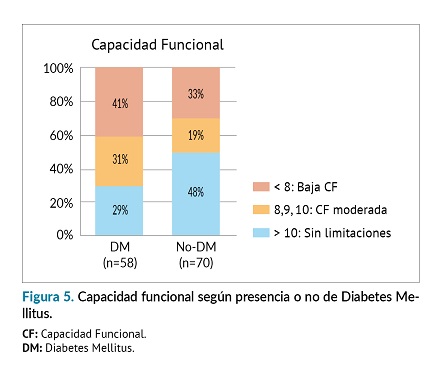
En la batería SPPB, el 37% (n=47) de los pacientes resultaron obtener baja capacidad funcional, el 24% (n=31) moderada y el 39% (n=50) resultaron sin limitaciones. Se observó mayor porcentaje de bajo rendimiento en el grupo de pacientes diabéticos (41% DM vs 33% no DM) y mayor porcentaje de pacientes autónomos en los no diabéticos (p=0,026) (figura 5).
Según el análisis de correlaciones de la totalidad de la muestra analizada en este estudio, la fragilidad mostró una relación directa con la edad (r=0,550; p<0,001), la comorbilidad (r=0,566; p<0,001), el grado de dependencia para las ABVD (r=0,615; p<0,001) y las AIVD (r=0,578; p<0,001), el riesgo de caídas (r=0,540; p<0,001) y la capacidad funcional medida por SPPB (r=0,612; p<0,001). Estas correlaciones se mantuvieron al estratificar entre los grupos de diabéticos y no diabéticos.
DISCUSIÓN
Los datos obtenidos en este estudio ponen de manifiesto, una vez más, la elevada prevalencia de fragilidad de las personas con ERC que realizan HD respecto a otros estudios llevados a cabo en población sin ERC16,17,24. Un estudio español de fragilidad realizado en Albacete a 1.172 participantes (FRADEA)24, halló una prevalencia de fragilidad del 16,9% en personas mayores de 70 años sin ERC, dato sensiblemente inferior al hallado en nuestro estudio. Lee et al.17 informaron en su estudio en Corea del Sur una prevalencia de fragilidad de pacientes en HD del 34,8%, siendo sustancialmente más elevada que la hallada en la población sin ERC. La revisión sistemática de Chowdhury et al.16 también demostró la elevada prevalencia de fragilidad en pacientes con ERC y que aquellos en estadíos más avanzados de la enfermedad tenían más probabilidades de ser frágiles. Estos estudios asociaron la fragilidad con mayor riesgo de hospitalización y mayor morbi-mortalidad16,17.
Analizando los resultados por franjas de edad, observamos un notable aumento de la fragilidad según avanza la edad, sin menospreciar los resultados obtenidos en los pacientes más jóvenes, hallándose fragilidad en el 7% y pre-fragilidad en el 33% de nuestros pacientes menores de 65 años. Johansen et al.25 también hallaron en su cohorte de 2.275 pacientes en HD que una proporción significativa de éstos en los grupos de edad más jóvenes (el 44% de los menores de 40 años y el 61% de 40-50 años) también eran frágiles. La elevada prevalencia de fragilidad en personas con ERC respecto a la población general llevó al autor Simon R. Walker26 a proponer la ERC como un modelo para el envejecimiento acelerado, en el que están implicados el aumento de las toxinas urémicas, la inflamación, el estrés oxidativo, las endocrinopatías y el desgaste proteico-energético propios de la enfermedad renal.
Por lo tanto, parece que las personas con ERC tienen una mayor predisposición a desarrollar fragilidad, así como un mayor riesgo de padecer eventos adversos de salud de manera más temprana que los mayores sin ERC, más aún si cabe, si están en tratamiento con HD16,17. Debido a ello, detectar a estos pacientes frágiles es un objetivo, ya que la fragilidad se asocia con resultados de salud deficientes16. No sólo deberemos tener en cuenta a los pacientes frágiles, también a los pre-frágiles dado que, según el estudio FRADEA24, éstos últimos tienen un riesgo aumentado de convertirse en frágiles a los 3 años.
La pregunta que nos planteamos a continuación fue la siguiente: ¿son los pacientes con diabetes más frágiles que los no diabéticos? Según nuestros datos, los pacientes diabéticos eran mayores y tenían más comorbilidad que los no diabéticos. Además, se observó una tendencia porcentual que indicó mayor fragilidad de los pacientes diabéticos frente a no diabéticos.
Estos resultados están en la línea de los obtenidos por otros autores11,27,28. Johansen et al.27, en su estudio con una cohorte de 771 pacientes en tratamiento con HD observaron que, además de la edad y el sexo femenino, las personas con DM eran más propensas a ser frágiles. Kakio et al.28 también hallaron en su estudio una estrecha relación entre fragilidad y DM en pacientes sometidos a HD, en el que la prevalencia de fragilidad del grupo con DM fue significativamente mayor que en el grupo sin DM (28% vs 16,5%, p=0,0161). Según Navarrete-Reyes et al.11 las personas con DM tienen un peor desempeño muscular debido a la resistencia a la insulina, la neuropatía diabética, la disminución de hormonas anabólicas (testosterona) y el aumento de citocinas proinflamatorias. Todo esto contribuye a la disminución de la fuerza y la masa muscular, lo que favorece el desarrollo de fragilidad11. Al hilo de esta afirmación, los autores Formiga y Rodríguez19 explican en su editorial que la pérdida de peso frecuente en los pacientes con DM, el mal control glucémico (hemoglobina glicosilada >8,0%), la mayor duración de la DM (>6 años) y la pobre actividad física se asocian a disminución de la velocidad en la marcha y a pérdida de masa y fuerza muscular (sobre todo en las extremidades inferiores) y ésto se asocia a fragilidad. Concluyen afirmando que un paciente con DM no es más frágil por el simple hecho de padecer la enfermedad, pero sí debe ser considerado de alto riesgo para desarrollar fragilidad. En el metanálisis de Hyeon Ju-Lee17 se expone que los pacientes diabéticos tienen un mayor riesgo de fragilidad debido a la combinación de neuropatía, deterioro de la función cognitiva resultante de una enfermedad cerebrovascular, mecanismos de inflamación y pérdida de la capacidad de autocuidado.
Según los resultados obtenidos en la presente investigación respecto a la dependencia para las actividades de la vida diaria, un 31% de nuestros pacientes en HD tienen una puntuación por debajo de 90 en la escala de Barthel, es decir, tienen una dependencia moderada, severa o total para las ABVD y un 21% tienen dependencia moderada, grave o total para las AIVD. Aunque de manera no significativa, los pacientes diabéticos resultaron ser más dependientes para las AVD en ambas escalas (Barthel y Lawton). La pérdida de autonomía en población de edad avanzada en HD se ha relacionado en el estudio de Cook et al.18 con hospitalizaciones más frecuentes y prolongadas y una mayor morbi-mortalidad de esta población. Esta pérdida de autonomía, ya sea para el autocuidado personal o para la realización de las tareas del hogar tiene una repercusión directa en el funcionamiento de las unidades de HD, ya que los pacientes más dependientes van a requerir, por parte del personal sanitario, unos cuidados de enfermería específicos y una vigilancia más cuidadosa durante las sesiones de HD29. En Canadá se realizó un estudio de 162 pacientes en HD que sugirió que la mayoría de los pacientes de edad avanzada en HD tienen discapacidad para el autocuidado debido a altos niveles de comorbilidad, polifarmacia y marcadores de fragilidad, como déficits en la movilidad y fuerza18. Por lo tanto, realizar valoraciones para medir el grado de dependencia para realizar actividades básicas (tanto en el autocuidado como en el hogar) nos pueden ayudar a identificar a aquellos pacientes que corren riesgo de deterioro funcional en nuestras unidades, debiendo poner especial atención en los pacientes con DM.
Respecto al riesgo de caídas, los resultados de este estudio determinan que el 13% de los pacientes de nuestra unidad de HD tienen riesgo elevado de sufrir caídas, siendo sensiblemente superior en los pacientes diabéticos, las mujeres y los pacientes más frágiles por criterios de Fried. De éstos últimos, un 37,5% presenta riesgo elevado de sufrir caídas frente al 89% de los no frágiles que presentan riesgo bajo. Un estudio realizado en Brasil a 230 pacientes en HD halló que el 37,4% de los pacientes tenían un riesgo elevado de caídas y que factores relacionados como la DM o la necesidad de asistencia para caminar aumentaba la ocurrencia de caídas, pero no encontraron diferencias estadísticamente significativas de mayor riesgo de caídas en los pacientes frágiles vs los pacientes no frágiles30. Contrariamente a dicho estudio, nuestros resultados sí muestran una relación estadísticamente significativa entre fragilidad y riesgo de caídas, coincidiendo con el estudio de Mc Adams et al 31 en el que se demostró que los pacientes frágiles en HD tenían un riesgo de caídas tres veces superior a aquellos que no eran frágiles.
Los resultados de la prueba de capacidad funcional realizada mediante SPPB muestran que el 37% de nuestros pacientes tienen limitaciones severas en su capacidad funcional, observándose mayor porcentaje de pacientes sin limitaciones entre los no diabéticos y mayor porcentaje de diabéticos entre los que presentan peor capacidad funcional. Por otro lado, comentar que el 73% de los pacientes frágiles tienen una prueba SPPB por debajo de los 8 puntos. La ERC impulsa el deterioro de la capacidad funcional de las personas que la padecen y el test SPPB parece una herramienta útil para detectar este deterioro. Reese et al.14, utilizando datos de una cohorte de 3.939 adultos con ERC mostró que la puntuación de la SPPB disminuye con el empeoramiento de la función renal; individuos con tasa de filtrado glomerular (TFG) inferior a 60 ml/min tenían una puntuación de SPPB más baja que aquellos con TFG superior a 60 ml/min. Más recientemente, Nogueira et al.32 confirman el SPPB como test de elección para valorar la capacidad funcional en pacientes con ERC.
Analizando nuestros resultados por sexo, las mujeres han resultado ser más frágiles, más dependientes para las ABIVD y tienen mayor riesgo de caídas que los hombres. Los autores Lee y Son17 explican este hecho en su metaanálisis por las múltiples deficiencias hormonales anabólicas que padecen las mujeres mayores, de las cuales la disminución de los niveles de testosterona se correlaciona con fragilidad.
A la vista de nuestros resultados parece evidente la necesidad de implantar una valoración sistemática de la fragilidad.
Una de las dificultades que encontramos fue decidir qué instrumento utilizar para la medición de la fragilidad (dada la gran variedad desarrollada en los últimos años). La elección de uno u otro puede crear distorsión para la generalización de los resultados. Investigar en la literatura nos abre un abanico de posibilidades en el que podemos encontrar desde las escalas descritas inicialmente, hasta las más recientes, como calculadoras de fragilidad o aplicaciones para móviles.
Para este estudio se decidió utilizar el Fenotipo de fragilidad de Fried por ser una herramienta validada para población con ERC, aporta criterios objetivos, es fácilmente aplicable en la práctica diaria y disponíamos del material necesario para su realización (dinamómetro).
Este instrumento combinado con escalas habitualmente utilizadas de dependencia y caídas, junto con una sencilla valoración funcional (SPPB), nos orientan de forma rápida hacia el estado de fragilidad de un paciente en diálisis, debiendo poner especial énfasis y atención, como muestran nuestros resultados, en la población con DM.
Teniendo en cuenta lo explicado anteriormente y dado el progresivo envejecimiento de la población, así como la elevada prevalencia de la ERC y la DM, la previsión para el futuro es que se incluya a un número cada vez mayor de personas de edad avanzada con diabetes y otras comorbilidades en los programas de HD. El personal sanitario al cuidado del paciente en HD debería, cada vez más, incluir la detección temprana y sistemática de fragilidad en su práctica diaria. Esto nos va a ayudar a identificar a aquellas personas más susceptibles de desarrollar dependencia y establecer un plan terapéutico individualizado para retrasar su evolución, como inclusión en programas de actividad física, asesoramiento dietético, atención psicológica u otras actividades que den respuesta a las nuevas necesidades asistenciales y así mantener la autonomía del paciente durante más tiempo.
Nuestro estudio tiene varias limitaciones. Una de ellas es el tamaño reducido de la muestra. Otra de las limitaciones es que, al plantearse como un estudio transversal, no podremos valorar la evolución en el tiempo de la fragilidad y el estado funcional de nuestros pacientes, por lo que sería interesante realizar estudios longitudinales.
Aún así, hemos corroborado la elevada prevalencia de fragilidad de la población en diálisis respecto a la población general. Esta fragilidad aumenta progresivamente según avanza la edad y es más frecuente en mujeres que en hombres.
Actualmente cada vez son más los estudios de fragilidad en los pacientes en HD, pero son escasos los que, además, analicen la situación del paciente diabético en HD.
Con los datos analizados en este estudio podemos aportar que la subpoblación de pacientes con DM, probablemente al ser de mayor edad, tener una mayor comorbilidad, así como una peor capacidad funcional, un mayor grado de dependencia y un riesgo de caídas aumentado, son más propensos a ser más frágiles que los no diabéticos, reforzando la necesidad de objetivar la fragilidad de esta población en la práctica clínica diaria.
Agradecimientos
Nuestro más sincero agradecimiento a todos los pacientes que decidieron participar en este estudio, a todos los compañeros y compañeras del equipo de enfermería y fisioterapia que han colaborado en la recogida y cumplimentación de datos y al equipo médico del DIRAC por la ayuda prestada, sin todos ellos no habría sido posible.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Financiación
Los autores declaran no haber recibido financiación alguna.
BIBLIOGRAFÍA
1. Otero A, de Francisco A, Gayoso P, García F, EPIRCE Study Group. Prevalence of chronic renal disease in Spain: results of the EPIRCE study. Nefrologia 2010;30(1):78-86.
2. Gorostidi M, Sánchez-Martínez M, Ruilope LM, Graciani A, de la Cruz JJ, Santamaría R, et al. Prevalencia de enfermedad renal crónica en España: impacto de la acumulación de factores de riesgo cardiovascular. Nefrologia 2018;38(6):606-15.
3. Registro español de enfermos renales (REER). Informe 2020 (Datos preliminares). 51 Congreso virtual de la Sociedad Española de Nefrología (SEN) [Internet] 2021 [consultado 11 Sep 2022]. Disponible en: https://www.senefro.org/contents/webstructure/MEMORIA_REER_2020_PRELIMINAR.pdf.
4. Beltrán Catalán S, Górriz Teruel J., Pallardó Mateu L. Hemodiálisis en pacientes con diabetes: indicaciones, ventajas y posibles complicaciones. Av en Diabetol 2010;26(4):248-52.
5. Zingerman B, Korzets A, Ori Y, Herman-Edelstein M, Rozen-Zvi B, Gafter U CA. The very old on hemodialysis: 8 years’ experience in a single unit. Blood Purif 2014;37(1):12-7.
6. Portilla Franco ME, Tornero Molina F, Gil Gregorio P. La fragilidad en el anciano con enfermedad renal crónica. Nefrologia 2016;36(6):609-15.
7. Lee So-Young, Yang DH, Hwang E, Kang SH, Park SH, Kim T, et al. The Prevalence, Association, and Clinical Outcomes of Frailty in Maintenance Dialysis Patients. J Ren Nutr 2017;27(2):106-12.
8. Li Y, Zhang D, Ma Q, Diao Z, Liu S, Shi X. The impact of frailty on prognosis in elderly hemodialysis patients: A prospective cohort study. Clin Interv Aging 2021;16:1659-67.
9. Tornero F, Portilla ME, Tornero FJ, Herrero JA. Fragilidad y Sarcopenia en la Enfermedad Renal Crónica. Nefrol al día [Internet]. 2020 [consultado 21 Sep 2021]. Disponible en: https://www.nefrologiaaldia.org/es-articulo-fragilidad-sarcopenia-enfermedad-renal-cronica-356.
10. Morley JE, Vellas B, Abellan van Kan G, Anker E, Bauer JM, Bernabei R, et al. Frailty Consensus: A Call to Action. J Am Med Dir Assoc 2013;14(6):392-7.
11. Navarrete-Reyes AP, Ávila-Funes JA. Diabetes mellitus y el síndrome de fragilidad en el anciano. Rev Investig Clin [Internet]. 2010 [consultado 27 Abr 2019];62(4):327-32. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/21222312.
12. Oberg-Higgins BP, McMenamin E, Lee Lucas F, McMonagle E, Morrow J, Ikizler T. et al. Increased prevalence of oxidant stress and inflammation in patients with moderate to severe chronic kidney disease. Kidney Int 2004;65(3):1009-16.
13. Toyoda K, Ninomiya T. Stroke and cerebrovascular diseases in patients with chronic kidney disease. Lancet Neurol 2014;13(8):823-33.
14. Reese PP, Cappola AR, Shults J, Townsend RR, Gadegbeku C, Anderson C, et al. Physical performance and frailty in chronic kidney disease. Am J Nephrol 2013;38(4):307-15.
15. López-Soto PJ, De Giorgi A, Senno E, Tiseo R, Ferraresi A, Canella C, et al. Renal disease and accidental falls: A review of published evidence. BMC Nephrol 2015;16(1).
16. Chowdhury R, Peel NM, Krosch M, Hubbard RE. Frailty and chronic kidney disease: A systematic review. Arch Gerontol Geriatr 2017;68:135-42.
17. Lee H-J, Son Y-J. Prevalence and Associated Factors of Frailty and Mortality in Patients with End-Stage Renal Disease Undergoing Hemodialysis: A Systematic Review and Meta-Analysis. Int J Environ Res Public Health 2021;18(7):3471.
18. Cook WL, Jassal SV. Functional dependencies among the elderly on hemodialysis. Kidney Int 2008;73(11):1289-95.
19. Formiga F, Rodríguez Mañas L. Paciente anciano con diabetes mellitus y fragilidad. ¿Asociación siempre presente? Rev Esp Geriatr Gerontol 2014;49(6):253-4.
20. Iglesias P, Heras M, Díez JJ. Diabetes mellitus y enfermedad renal en el anciano. Nefrologia 2014;34(3):285-92.
21. Fried LP, Tangen CM, Walston J, Newman A, Hirsch C, Gottdiener J, et al. Frailty in Older Adults: Evidence for a Phenotype. J Gerontol Med Sci Am 2001;56(3):146-56.
22. Johansen K, Delgado C, Bao Y, Kurella Tamura M. Frailty and dialysis initiation. Semin Dial 2013; 26(6):690-6.
23. Bancu I, Graterol F, Bonal J, Fernández-Crespo P, García J, Aguerrevere S, et al. Frail Patient in Hemodialysis: A New Challenge in Nephrology—Incidence in Our Area, Barcelonès Nord and Maresme. J Aging Res 2017;2017:1-5.
24. Abizanda P, López-Torres J, Romero L, López M, Sanchez PM, Atienzar P, et al. Fragilidad y dependencia en Albacete (estudio FRADEA): razonamiento, diseño y metodología. Rev Esp Geriatr Gerontol 2011;46(2):81-8.
25. Johansen KL, Chertow GM, Jin C, Kutner NG. Significance of Frailty among Dialysis Patients. J Am Soc Nephrol 2007;18(11):2960-7.
26. Walker SR, Wagner M, Tangri N. Chronic Kidney Disease, Frailty, and Unsuccessful Aging: A Review. J Ren Nutr 2014;24(6):364-70.
27. Johansen KL, Dalrymple LS, Delgado C, Chertow GM, Segal MR, Chiang J, et al. Factors Associated with Frailty and Its Trajectory among Patients on Hemodialysis. Clin J Am Soc Nephrol 2017;12(7):1100-8.
28. Kakio Y, Uchida HA, Takeuchi H, Okuyama Y, Okuyama M, Umebayashi R, et al. Diabetic nephropathy is associated with frailty in patients with chronic hemodialysis. Geriatr Gerontol Int 2018;18(12):1597-602.
29. Arenas MD, Álvarez-Ude F, Angoso M, Berdud I, Antolin A, Lacueva J, et al. Valoración del grado de dependencia funcional de los pacientes en hemodiálisis (HD): Estudio multicéntrico. Nefrologia 2006;26(5):600-8.
30. Carvalho TC de, Dini AP. Risk of falls in people with chronic kidney disease and related factors. Rev Lat Am Enfermagem 2020;28:e3289.
31. McAdams-DeMarco MA, Suresh S, Law A, Salter ML, Giménez LF, Jaar BG, et al. Frailty and falls among adult patients undergoing chronic hemodialysis: a prospective cohort study. BMC Nephrol 2013;14(1):224.
32. Nogueira Á, Álvarez G, Russo F, San-José B, Sánchez-Tomero JA, Barril G. ¿Es útil el SPPB como método de screening de capacidad funcional en pacientes con enfermedad renal crónica avanzada? Nefrologia 2019;39(5):489-96.
Este artículo se distribuye bajo una Licencia Creative Commons Atribución–NoComercial 4.0 Internacional.
https://creativecommons.org/licenses/by-nc/4.0/
